Categoría: Sesiones Médicas
Papel de los fármacos mucoactivos en el tratamiento de la enfermedad pulmonar obstructiva crónica
Las secreciones de tráquea y bronquios contribuyen significativamente a los síntomas de la enfermedad pulmonar obstructiva crónica. Se trata de un criterio diagnóstico de bronquitis crónica y una de las principales causas de obstrucción del flujo aéreo. Además, la hipersecreción de moco crónica se asocia con un aumento de la mortalidad y una disminución acelerada del volumen respiratorio forzado en el primer segundo (VEF1), y un mayor riesgo de hospitalización en la enfermedad pulmonar obstructiva crónica.
Los medicamentos mucoactivos, son fármacos con la capacidad de modificar la producción de moco, la secreción, su naturaleza y composición, o sus interacciones con el epitelio mucociliar.
Propiedades del moco
El líquido de la superficie que cubre el revestimiento epitelial de las vías respiratorias comprende al menos dos capas: la capa de moco (gel) y la capa acuosa periciliar (que rodea los cilios). El moco se compone de una mezcla de fluido y secreciones de trasudado del epitelio de la superficie y las glándulas mucosas. Se compone fundamentalmente de:
- Agua en un 95%
- Glicoproteínas de 2 a 3%
- Proteoglicanos (0.3 a 0.5%)
- Lípidos (0.3 a 0.5%)
- Proteínas y ADN.
El volumen normal de moco es aproximadamente 15 ml al día. La secreción de moco puede aumentar de tres veces en la enfermedad pulmonar obstructiva crónica y 10 veces en la fibrosis quística. La composición también puede cambiar en estados de enfermedad como por ejemplo el ADN puede aportar hasta 10% del peso seco del moco en la fibrosis quística.
El moco se comporta como un fluido no Newtoniano con propiedades visco-elásticas. Las propiedades viscosas (líquidas) permiten al moco que sea extruido por glándulas. Las propiedades elásticas, de tipo sólido permiten la transferencia, almacenamiento y la conversión de la energía impartida por los cilios. Las glicoproteínas son esenciales para la elasticidad de la mucosidad.
Para determinar la capacidad de un agente para promover la eliminación de secreciones, es necesario abordar tanto un aclaramiento mucociliar y un aclaramiento de la tos (Es decir, las propiedades que regulan el flujo) se han reportado diferentes propiedades reológicas y potencialmente antagónicas entre estos dos mecanismos de transporte de moco. Por ejemplo, la eliminación del moco requiere la transferencia eficaz de energía cinética de los cilios hacia el moco. Los factores que mejoran el transporte del moco incluyen: una mayor elasticidad de moco (para almacenar la energía transmitida), la viscosidad del moco inferior (para reducir la pérdida de energía), mayor adhesividad (que impide la formación de ondas en la capa de gel), aumento de la capacidad de hilado (una medida de la capacidad de formación de hilo de moco), aumento de la frecuencia de movimiento ciliar, una capa de disolvente de moco, y una solución ciliar mayor la altura de los cilios (para mejorar el acoplamiento con puntas ciliares).
En contraste, los factores que mejoran la limpieza por tos incluyen: una mayor viscosidad de moco, menor elasticidad de moco (para reducir el retroceso de moco), adhesividad inferior (para promover la formación de ondas en el gel), menor capacidad de hilado, una capa de moco grueso, y una capa de solución periciliar que es más alta que la altura de los cilios.
Los estados de enfermedad pueden afectar las propiedades reológicas del moco. Por ejemplo los niveles de mucinas formadoras de gel, MUC5A se y MUC5B, son elevadas en las vías respiratorias y el estudio de individuos con enfermedades respiratorias crónicas (EPOC), y pueden contribuir a las propiedades visco-elásticas de moco. Los pacientes con asma, parece tener la viscosidad más alta en el esputo, mientras que los pacientes con fibrosis quística tienen menor viscosidad. Los pacientes con bronquitis crónica y bronquiectasias tienen un esputo con viscosidad intermedia.

Fármacos con propiedades mucoactivas de uso rutinario en la EPOC.
Agonistas Beta: mejoran el aclaramiento del moco de las vías respiratorias en gran parte a través de un efecto sobre la frecuencia del movimiento ciliar.
Anticolinérgicos: Algunos agentes anticolinérgicos como la atropina reducen la secreción de saliva, lo que se traduce en una reducción significativa en la velocidad del moco traqueal y transporte mucociliar; sin embargo no parece tener efecto sobre la secreción de moco.
El Bromuro de Ipratropio no parece tener el mismo efecto que la Atropina, no hay estudios que demuestren que tenga efectos en la secreción de moco o en el movimiento mucociliar. De esta manera el Bromuro de Ipratropio parece mejorar la obstrucción de la vía aérea sin afectar negativamente el movimiento mucociliar. Estos efectos son similares a los del Tiotropio.
Metilxantinas: Las Metilxantinas estimulan el movimiento mucociliar e incrementan el flujo de agua hacia la luz de las vías respiratorias, estos efectos dependen de la dosis y de la irritación gástrica que producen (y así producción de secreción en las vías respiratorias por estimulo Vagal) además de su efecto broncodilatador.
La Aminoflina incrementa la depuración mucociliar en pacientes con EPOC, sin embargo este efecto no mejora la función pulmonar o disminuye la tos.
El papel de las Metilxantinas en el EPOC va relacionado a mejorar la tolerancia al ejercicio, mejorando la depuración de las secreciones y disminuyendo la frecuencia de las exacerbaciones.
Inhibidores de la Fosfodiesterasa
Los inhibidores de la Fosfodiesterasa 4 (Roflumilast), aunque no son agentes con propiedades mucoactivas, se ha encontrado que disminuye la frecuencia de las exacerbaciones del EPOC con fenotipo de Bronquitis Crónica.
Glucocorticoides inhalados
Los glucocorticoides inhalados pueden actuar como agentes mucorreguladores, disminuyendo la hipersecreción de moco, este beneficio parece estar relacionado al controlar la inflamación de la vía aérea, sin afectar la depuración mucociliar.
Estrategias mucoactivas para pacientes seleccionados
Antibióticos
Algunos antibióticos tienen efectos mucoactivos, efectos que van más allá de su efecto antimicrobiano, estos efectos incluyen: inhibición de las citocinas proinflamatorias o inmunomodulación de los efectos antiinflamatorios.
Estos cambios se han visto implicados en pacientes con exacerbaciones de su EPOC y están asociados a cambios en el volumen y color del esputo.
Los antibióticos son usados para disminuir la carga bacteriana que contribuye a la inflamación y al aumento en la producción de esputo, además los macrólidos pueden tener propiedades proinflamatorias que reducen la secreción de moco independientemente del efecto antimicrobiano. Un ejemplo seria el efecto benéfico que posee la eritromicina en la panbronquiolitis difusa, una patología en donde existe una producción copiosa de moco que disminuye considerablemente con el uso de este medicamento.
Los antibióticos macrólidos se ha encontrado que reducen la frecuencia de las exacerbaciones en ciertos pacientes con enfermedad pulmonar obstructiva crónica, aunque se debe seleccionar cuidadosamente al paciente y monitorearlo por posibles efectos adversos. La terapia de largo plazo con moxifloxacino también parece ser beneficiosa para pacientes con enfermedad pulmonar obstructiva crónica quienes tienen exacerbaciones frecuentes.
Tioles y derivados del Tiol
Estos agentes rompen los puentes disulfuro y actúan directamente sobre las mucoproteínas, la licuefacción del moco y la reducción de su viscosidad. Además pueden tener otras propiedades antiinflamatorias y antibacterianas.
N-Acetilcisteína: Licua la mucosidad y el ADN, tiene efectos antioxidantes cuando se usa una dosis adecuada. Sin embargo, no se utiliza de manera rutinaria en pacientes con EPOC, ya que existen revisiones sistemáticas que han encontrado poco o ningún beneficio en la reducción de exacerbaciones o mejora en la calidad de vida, sin embargo hay estudios que utilizan dosis elevadas que muestran un beneficio modesto.
Erdosteína: Es otro agente Tiol con un perfil de seguridad mayor y menores efectos secundarios que otros derivados de Tiol. Ha demostrado (EQUALIFE) una reducción de hasta 30% de las exacerbaciones y una reducción de 58 días la hospitalización por exacerbación aguda del EPOC. Además posee propiedades antiinflamatorias, niveles reducidos de leucotrienos.
Carbocisteina: Ha demostrado una reducción de las exacerbaciones y mejora de la calidad de vida a 12 meses (PEACE).
Los Tioles o derivados del Tiol, principalmente Erdosteína y Carbocisteina, son una opción para disminuir las exacerbaciones del EPOC en pacientes quienes por alguna razón no pueden utilizar Glucocorticoides inhalados con Agonistas beta de acción prolongada o agentes muscarínicos de acción prolongada, sin embargo no hay evidencia clara de que estos agentes reduzcan las exacerbaciones cuando se utilizan como tratamiento complementario a los tratamientos ya establecidos.

Agentes mucoactivos de actividad limitada o sin beneficio
Hidratación: Mientras se mantiene una hidratación normal las secreciones se mantienen con sus propiedades ya establecidas, no hay evidencia que la sobre-hidratación ofrezca algún beneficio para la producción de esputo.
Solución salina hipertónica: Se han utilizado tradicionalmente para inducir la expectoración de esputo para la evaluación diagnostica. Los efectos de la solución salina hipertónica incluyen:
- Estimulación de tos productiva
- Disminución de la capacidad de hilado del esputo
- Disminución de la visco-elasticidad del esputo
Existe evidencia de los efectos benéficos en la Fibrosis quística de esta terapéutica, sin embargo la evidencia es limitada en la EPOC. Además los aerosoles de solución hipertónica o isotónica pueden inducir una disminución de la función pulmonar en pacientes con EPOC debido a la broncoconstricción. Este efecto puede estar mediado por mastocitos, ya que la disminución de la función pulmonar es más pronunciada en pacientes con histamina en el esputo.
Expectorantes orales: tales como la guaifenesina, bromhexina, ipecacuana, sales de amonio, estimulan el nervio gástrico y promueven la secreción de las vías respiratorias por una estimulación del nervio vago. Además reducen la viscosidad del moco, y aumentan el ascensor mucociliar.
Sin embargo no hay estudios clínicos que establezcan que existe mejoría al usar estos agentes en la EPOC.
Preparaciones de yodo: El yoduro actúa como mucolítico disminuyendo la viscosidad del moco, facilitando la descomposición de las proteínas por enzimas proteolíticas, y aumentando la frecuencia del movimiento ciliar.
Preparaciones de yodo incluyen solución saturada de yoduro de potasio (SSKI), domiodol, y Iodopropilideno Glicerol. Debido a su perfil de efectos adversos, no se recomiendan para su uso como agentes mucolíticos en la EPOC.
Cromoglicato de sodio: El cromoglicato de sodio puede mejorar la velocidad del moco traqueal deprimida en los asmáticos.
ADN-asa Recombinante humana: El ADN liberado por los leucocitos se cree que contribuyen significativamente a la viscosidad del moco en pacientes con fibrosis quística (FQ). Se considera un agente mucocinético que puede producir mejoría de la función pulmonar en pacientes con FQ clínicamente estables. Sin embargo, la ADN-asa recombinante humana no parece ser eficaz en el tratamiento de la bronquiectasia no relacionada con la FQ y se carece de datos respecto a su uso en la EPOC.
Referencias
- Meyer T, Reitmeir P, Brand P, et al. Effects of formoterol and tiotropium bromide on mucus clearance in patients with COPD. Respir Med 2011; 105:900.
- Rennard SI, Calverley PM, Goehring UM, et al. Reduction of exacerbations by the PDE4 inhibitor roflumilast–the importance of defining different subsets of patients with COPD. Respir Res 2011; 12:18.
- Global Initiative for Chronic Obstructive Lung Disease. Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Lung Disease. http://www.goldcopd.org (Noviembre 2 del 2014).
- National Clinical Guideline Centre. (2010) Chronic obstructive pulmonary disease: management of chronic obstructive pulmonary disease in adults in primary and secondary care. London: National Clinical Guideline Centre. http://guidance.nice.org.uk/CG101/Guidance/pdf/English (Noviembre 2, 2014).
- Zheng JP, Wen FQ, Bai CX, et al. Twice daily N-acetylcysteine 600 mg for exacerbations of chronic obstructive pulmonary disease (PANTHEON): a randomised, double-blind placebo-controlled trial. Lancet Respir Med 2014; 2:187.
- Zheng JP, Kang J, Huang SG, et al. Effect of carbocisteine on acute exacerbation of chronic obstructive pulmonary disease (PEACE Study): a randomised placebo-controlled study. Lancet 2008; 371:2013.
- Role of mucoactive agents in the treatment of COPD. 2011. http://www.uptodate.com/contents/role-of-mucoactive-agents-in-the-treatment-of-copd (Noviembre 2 del 2014)
Trastorno Depresivo Mayor
La depresión es un síndrome caracterizado por abatimiento del humor asociado a síntomas somáticos, cognoscitivos y vegetativos, que impactan en el funcionamiento social laboral y/o académico.
Epidemiología
La prevalencia del trastorno presenta una media de 10%, con una relación hombre:mujer de 1:2. En México, en 2003, los resultados mostraron una tasa de prevalencia de 2 y 4.5% en hombres y mujeres, respectivamente, con un episodio depresivo mayor a lo largo de la vida de la población en general de 3.3%.
Fisiopatología
Se asocia alteraciones genéticas y a alteraciones en los neurotransmisores, principalmente serotonina, norepinefrina, dopamina, entre otros.
Alteraciones en la neurotransmisión
Serotonina: Está implicada en la regulación del ciclo sueño-vigilia, el apetito, la conducta sexual y la agresión. Los resultados de los estudios neuroendocrinológicos sugieren una disminución de la neurotransmisión serotoninérgica. Muchos antidepresivos actuarían aumentando los niveles de serotonina a través de una disminución de su recaptación en las sinapsis.
Noradrenalina. Desempeña un papel importante en el man- tenimiento de la activación y el impulso. El sistema noradrenérgico se ha involucrado en la etiología de los trastornos depresivos, y prueba de ello es la regulación a la baja de los receptores alfa-2 somatodendríticos producida por los antidepresivos.
Dopamina. Se ha observado una disfunción dopaminérgica en la depresión psicótica, la bipolar, el trastorno afectivo estacional y la depresión asociada a la enfermedad de Parkinson. Los antidepresivos podrían resolver la anhedonía y la pérdida de impulso incrementando la sensibilización de los receptores dopaminérgicos D2 y D3.
Factores de riesgo de depresión son:
a) Historia familiar de enfermedad mental.
b) Trastornos crónicos físicos o mentales (infartos cerebrales, infartos
miocárdicos, cáncer, etcétera).
c) Cambios mayores de vida y estrés.
d) Ausencia de apoyo psicológico.
e) Dificultades económicas.
f) Edad avanzada.
g) Insomnio.
h) Medicamentos (analgésicos, sedantes, hipnóticos, esteroides).
Manifestaciones clínicas
- Ansiedad
- Falta de concentración
- Ánimo bajo
- Anergia
- Anhedonia
- Ideas autoliticas
- Pesimismo
- Baja autoestima
- Alteraciones del sueño y/o del apetito
- Sentimientos de culpa
El paciente depresivo tiene una postura encorvada, sus movimientos espontáneos están muy restringidos y su mirada es la de una persona abatida.
Diagnóstico
El episodio depresivo se diagnostica con la información obtenida a través de la entrevista clínica, ya que no existen marcadores biológicos útiles para el diagnóstico.
Criterios DSM-IV
| Criterios diagnósticos generales de episodio depresivo según CIE-10 |
| A. El episodio depresivo debe durar al menos dos semanas. |
| B. El episodio no es atribuible a abuso de sustancias psicoactivas o a trastorno mental orgánico. |
C. Síndrome Somático: comúnmente se considera que los síntomas “somáticos» tienen un significado clínico especial y en otras clasificaciones se les denomina melancólicos o endógenomorfos
|
| Fuente: Adaptado de OMS. Décima Revisión de la Clasificación Internacional de Enfermedades. CIE-10. |
| Criterios de gravedad de un episodio depresivo según CIE-10 |
A. Criterios generales para episodio depresivo
|
B. Presencia de al menos dos de los siguientes síntomas:
|
C. Además debe estar presente uno o más síntomas de la siguiente lista, para que la suma total sea al menos de 4:
|
| D. Puede haber o no síndrome Somático
Según estos criterios, podemos clasificarlo:
|
- Episodio depresivo moderado: Están presentes al menos dos síntomas del criterio B y síntomas del criterio C hasta sumar un mínimo de 6 síntomas. La persona con un episodio moderado probablemente tendrá dificultades para continuar con sus actividades ordinarias.
- Episodio depresivo grave: Deben existir los 3 síntomas del criterio B y síntomas del criterio C con un mínimo de 8 síntomas. Las personas con este tipo de depresión presentan síntomas marcados y angustiantes, principalmente la pérdida de autoestima y los sentimientos de culpa e inutilidad. Son frecuentes las ideas y acciones suicidas y se presentan síntomas somáticos importantes. Pueden aparecer síntomas psicóticos tales como alucinaciones, delirios, retardo psicomotor o estupor grave. En este caso se denomina como episodio depresivo grave con síntomas psicóticos. Los fenómenos psicóticos como las alucinaciones o el delirio pueden ser congruentes o no congruentes con el estado de ánimo.
Fuente: OMS. Décima Revisión de la Clasificación Internacional de Enfermedades. CIE-10.
Cuestionarios Diagnósticos
Uno de los métodos de evaluación más empleados son los cuestionarios. Son instrumentos cuyo objetivo es realizar un registro de los sentimientos e ideas recientes, así como hacer un repaso, más o menos exhaustivo, sobre las distintas áreas/dimensiones que pueden estar afectadas: afectiva, conductual y/o fisiológica.
Los cuestionarios de evaluación de la depresión tienen diferentes utilidades: cuantificar la intensidad de la sintomatología, establecimiento de áreas conductuales problemáticas, detección de cambios sintomatológicos (monitorización de síntomas), realizar cribado e incluso, cualificar el tipo de trastorno.
Las características operativas entre un cuestionario y otro no difieren mucho, aunque varían considerablemente en los estudios alcanzando una sensibilidad entre 50-97% (media 85%) y una especificidad entre 51-98% (media 74%). Estos cuestionarios tienen entre 15 y 30 preguntas, aunque versiones mas cortas (entre 2 y 9 preguntas) han demostrado una utilidad similar, con una sensibilidad y especificidad ligeramente más bajas.
GDS-5: Es la versión de 5 preguntas de la GDS y que ha sido validada para adultos mayores y para adultos jóvenes. Una puntuación de 2 o más nos da positividad ante depresión.
Two-ítem screening tool: Es una sola pregunta: ^¿Esta deprimido?^
O dos preguntas que evalúan depresión y anhedonia:
- ¿Durante el mes pasado se ha sentido decaído, deprimido o sin esperanza?
- ¿Durante el mes pasado ha sentido poco interés o lacer al hacer las cosas?
PHQ-2: Es un test similar que evalúa depresión y anhedonia en las 2 semanas previas a la consulta medica.
PHQ-9: Es un test que evalúa los 9 síntomas que establece el DSM-IV para el diagnostico de depresión mayor. Establece el diagnostico de depresión y no requiere confirmación.
Beck Depression Inventory for Primary Care: Es un cuestionario de 7 preguntas que es una adaptación del cuestionario de 21 preguntas, tiene 97 y 99% de sensibilidad y especificidad respectivamente para detectar depresión mayor.
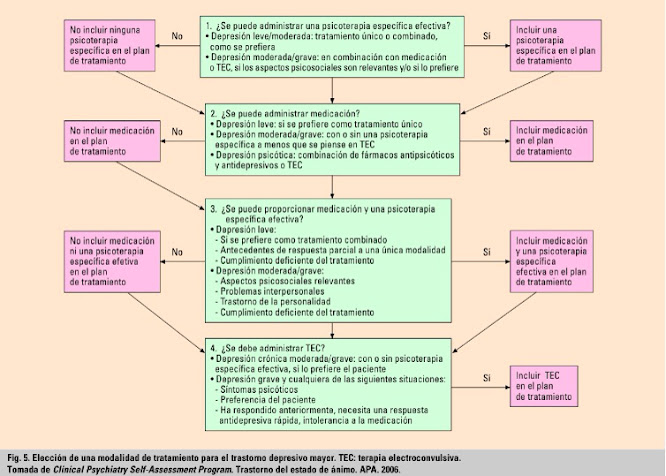
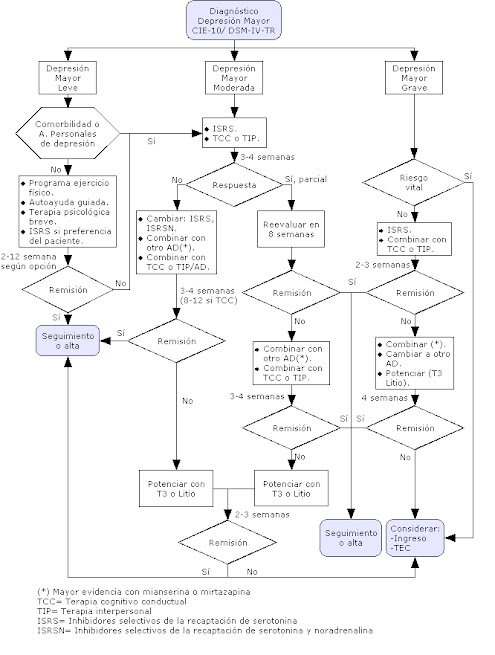
Tratamiento
El objetivo del tratamiento es conseguir tanto la remisión del episodio agudo como la prevención de las recurrencias de la enfermedad y consta de tres fases:
1. Fase aguda: el objetivo es inducir la remisión y su duración varía entre las seis y las ocho semanas.
2. Fase de continuación: el objetivo es conservar la remisión y su duración varía entre las 16-20 semanas.
3. Fase de mantenimiento: el objetivo es proteger al paciente de la recurrencia de episodios depresivos posteriores. Su duración depende de la frecuencia y la gravedad de los episodios depresivos previos.
Distimia
La distimia, término introducidopor primera vez en la tercera edi-ción del DSM, es una entidaddiagnóstica heterogénea que en-globa a aquellos trastornos del estado de ánimo depresivos, insidiosos y de curso crónicoque no alcanzan la intensidad suficiente para cumplir los cri-terios diagnósticos anteriormente expuestos de episodio de-presivo mayor. Son pues depresiones clínicamente inestablesy mal definidas.
Referencias:
Medicine. 2007;09:5451-60. – vol.09 núm 85
Dislipidemias
Termino que abarca una serie de trastornos caracterizados por cambios en las concentraciones séricas de lípidos, aumento o disminución de los mismos.
Metabolismo de los lípidos
Funciones de los lípidos:
- Almacenamiento de energía
- Forman parte de membranas celulares
- Estructura de hormonas
- Estructura de vitamina D
- Estructura de mediadores interceluláres
Los lípidos son hidrofóbicos, por lo cual necesitan de proteínas que les transporten en el torrente circulatorio, las lipoproteinas. Se reconocen 5 tipos de lipoproteinas:
- Quilomicrones (Q)
- Lipoproteínas de muy baja densidad (VLDL)
- Lipoproteínas de densidad intermedia (IDL)
- Lipoproteínas de baja densidad (LDL)
- Lipoproteínas de alta densidad (HDL)
Estas lipoproteínas están compuestas por los siguientes elementos:
Lípidos: Colesterol, triglicéridos, fosfolípidos
Proteínas:
Apolipoproteínas (Apo):
- Apo A: Se sintetizan en hígado e intestino, existen varias subclases Apo A1, Apo A2, entre otras. Se transfieren de forma activa entre los Quilomicrones (Q), HDL y VLDL.
- Apo A1: Su función principal es la de activar la Lecitín colesterol acil transferasa (LCAT), que esterifíca el colesterol de las HDL y en nivel periférico. También transloca el colesterol libre desde el interior de la célula hacia la membrana celular, con la participación de los transportadores de colesterol ABC A1 (ATP Binding Cassette A1)
- Apo B: se reconocen dos formas principales, la Apo B48 que es sintetizada en intestino y la Apo B100, sintetizada en Higado. La Apo B48 forma parte estructural de los Quilomicrones; mientras que la Apo B100 forma parte de las VLDL, IDL y LDL.
- Apo C: Sintetizada a nivel hepático, de la cual se reconocen tres subclases, C1, C2 y C3. La Apo C2 estimula a la lipoproteinlipasa (LPL) mientras que la C3 la inhibe.
- Apo E: Se sintetizan a nivel hepático, igualmente se reconocen tres subclases: E2, E3 y E4. También estimulan la transferencia intravascular entre HDL, VLDL y Quilomicrones, dirigiendo las lipoproteínas hacia los receptores hepáticos y periféricos.
Receptores:
Reconocemos receptores hepáticos y periféricos:
- Los receptores hepáticos son afines a Apo E: Receptor de remanentes de Quilomicrones (B48:E)
- Receptor de LDL relacionado con proteínas (LRP)
- Receptor compartido de los remanentes de VLDL y LDL (B100:E)
- Scavenger Receptor de HDL2 (SR-B1)
Enzimas:
- Lipoprotein lipasa (LPL): sintetizada en células y translocada a la pared vascular, activada por la Apo C2 e inhibida por la Apo C3. La insulina actúa como su cofactor. Actúa catabolizando los triglicéridos contenidos en Quilomicrones y VLDL.
- Lipasa lipoproteica hepática (LPLH): es regulada por la síntesis de colesterol a nivel hepático y su función es catabólica sobre los remanentes de Quilomicrones, VLDL y HDL2.
- Lecitín colesterol acil transferasa (LCAT): esterifíca el colesterol libre de las HDL, ya esterificada ocupa su interior. Estimulada por la Apo A1 y la Apo C1.
- Proteína transportadora de esteres de colesterol (CEPT) transporta el colesterol esterificado desde las HDL a VLDL, IDL y LDL; y de triglicéridos desde la VLDL a HDL y LDL.
Metabolismo normal
El transporte de los lípidos ocurre con dos destinos diferentes. La primera vía tiene el objetivo de transportar los lípidos desde los sitios donde se producen o absorben (Hígado e intestino respectivamente) hacia los tejidos donde se utilizan o almacenan (músculo, grasa, glándulas, etc). La segunda vía tiene como objetivo transportar los lípidos desde tejidos periféricos para su depuración hepática.
Lipoproteínas derivadas del intestino
Los lípidos ingeridos en la dieta son transportados al interior de los Quilomicrones, estas lipoproteinas contienen Apo A1, A2 y B48 y como componente lipídico contienen triglicéridos, colesterol y bilis, son absorbidas por vía linfática y en la circulación reciben Apo C y Apo E desde las HDL. Son hidrolizadas por la LPL de la pared vascular, liberando ácidos grasos y glicerol, quedando como Remanentes de Quilomicrones, los cuales transfieren Apo C y Apo A1 a las HDL. Posteriormente en hígado son captados estos remanentes por los receptores B48:E, continuando su catabolismo por la LPLH
Lipoproteínas derivadas del hígado
Los lípidos sintetizados en el hígado son transportados al interior de las VLDL, lipoproteínas sintetizadas en el hígado con Apo B100 y triglicéridos. En la circulación reciben Apo C y Apo E desde las HDL, después son hidrolizados por la LPL en la periferia. Posteriormente captados a nivel hepático por el receptor compartido de los remanentes (B100:E).
Las VLDL que ya pasaron por la LPL, pueden recibir colesterol de otras lipoproteínas por efecto de la CEPT, convirtiendose en IDL.
Estas IDL son degradadas por la LPLH, perdiendo la mayor cantidad de triglicéridos hasta contener casi exclusivamente colesterol, convirtiendose así en LDL. Estas LDL contienen Apo B100 y ricas en colesterol libre y esterificado, son captadas a nivel hepático por los receptores B100:E y por los receptores periféricos B100. Los receptores internalizan las LDL y permiten su catabolismo, liberando el colesterol que contienen que inhibe a la Hidroximetilglutaril Co A reductasa (HMGCoAR), enzima clave para la síntesis de colesterol.
El colesterol libre disminuye la síntesis de receptores B100 y B100:E y estimula a la acil colesterol acil transferasa, que esterifíca el colesterol, regulando así el contenido intracelular de este.
Lipoproteínas de alta densidad
Esta vía permite el transporte de lípidos de tejidos periféricos hacia el hígado, para ser eliminados. Se secretan y se sintetizan en el hígado e intestino a partir de preßHDL formadas por Apo A1 y fosfolipidos. Estas moléculas tienen la capacidad de atravesar el endotelio vascular de los tejidos y retiran el exceso de colesterol gracias al transportador de membrana ABCA1. Gracias a la LCAT el colesterol de la molécula es esterificado, e internalizado en la molécula, dejando espacio para captar mas colesterol, transformandose así en HDL3 y posteriormente en HDL2.
La depuración hepática de estas puede suceder por dos vías:
Por acción de la CEPT, transfieren el colesterol esterificado a VLDL y LDL, y estas lo llevan al hígado a través de los receptores B100:E
Por captación selectiva de colesterol a través del receptor SR-B1
Epidemiología
Según la Encuesta Nacional de Enfermedades Crónicas (ENEC), en 1993, donde se estudiaron a 13 274 pacientes entre 20 y 69 años; se demostró que la prevalencia de dislipidemia es alta en nuestro país. La concentración media de colesterol fue de 182.7 mg/dl, de LDL 116.6 mg/dl, de HDL 38.5 mg/dl y de triglicéridos 158.2 mg/dl.
Las hiperlipidemias más frecuentes informadas en la Encuesta Nacional de Enfermedades Cronicas fueron la hipertrigliceridemia y la hipoalfalipoproteinemia.
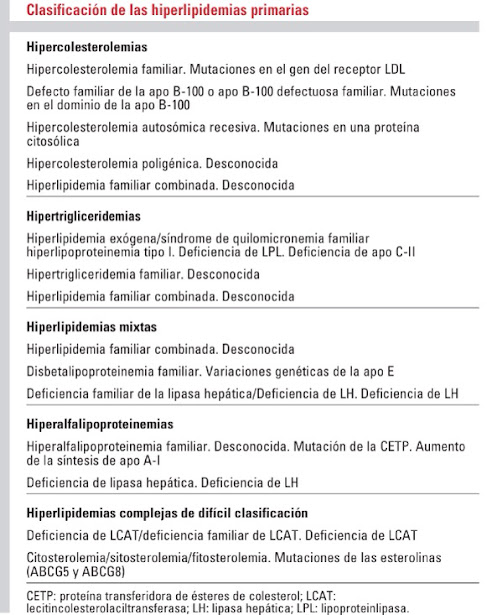
Clasificación
La clasificación mas conocida es la de fenotípica o de Fredrickson, pero ha caído en desuso porque no aporta información sobre su etiología; por otra parte, la clasificación genotípica las divide en primarias (Genéticas) y secundarias (enfermedades o fármacos) o mixtas.
Dislipidemias Primarias
Se denominan dislipidemias primarias a las elevaciones de las lipoproteínas plasmáticas debidas a causas genéticas.
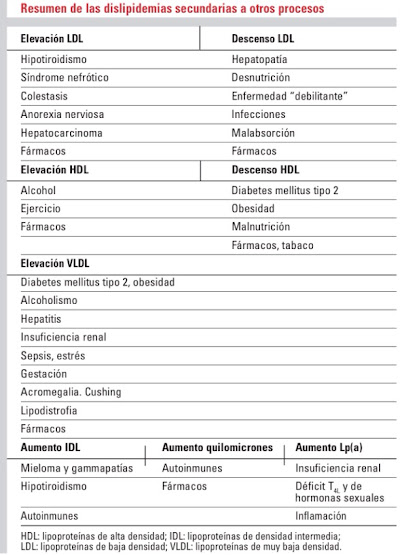
Dislipidemias Secundarias
Las dislipidemias secundarias incrementan la morbilidad de la enfermedad causal y pueden complicar una dislipidemia primaria.
Las dislipidemias secundarias pueden expresarse con diferentes perfiles lipídicos.
La dislipidemia secundaria más frecuente es la asociada a diabetes mellitus que puede mostrar cualquier tipo de perfil lipoproteico. El hipotiroidismo es la segunda causa de dislipidemia secundaria, y en él la alteración más frecuente es el colesterol LDL elevado.
Otras causas relevantes de hiperlipidemia secundaria que se expresan con fenotipos diferentes son:
Enfermedad renal
Consumo de alcohol
Hepatopatías crónicas y agudas
Obesidad
Síndrome de Cushing
Hipergammaglobulinemias
Fármacos como diuréticos tiacídicos
Glucocorticoides
Anticonceptivos orales
Bloqueadores beta
Inhibidores de la proteasa del virus de la inmunodeficiencia humana o ciclosporina.
Dislipidemias Mixtas
- Hiperlipidemia familiar combinada
- Disbetalipoproteinemia
Estudio del paciente con Dislipidemia
NCEP/ATP III recomienda el estudio a pacientes mayores de 20 años, con especial prioridad hacia aquellos que otros factores de riesgo cardiovascular, metabolicos o antecedentes heredofamiliares de Dislipidemias.
El estudio debe de incluir:
Colesterol Total
Triglicéridos
HDL
Estos parámetros permiten el calculo de C-LDL mediante la formula de Friedwald:
LDL= CT- (C-HDL=TG/5)
Esta formula no permite el calculo de LDL en aquellas personas que tienen TG >400mg/100 ml, en portadores de Diabetes Mellitus. En estos pacientes se recomienda la formula para obtener colesterol no-HDL:
No C-HDL= CT-C-HDL
Tratamiento
Tratamiento no Farmacologico
Habitos alimentarios sanos, ejercicio fisico, supresión del tabaco y bebidas alcohólicas, así como control de peso. En cuanto a la dieta, NCEP/ATP III recomienda que el porcentaje de calorías diarias de origen graso no supere el 30%; también recomienda el ejercico de tipo aerobico 30 minutos 5 veces por semana.
Tratamiento Farmacologico
Familias de Fármacos Hipolipemiantes
Estatinas. Son los hipocolesterolemiantes más eficaces y utilizados. Reducen la síntesis de colesterol, y además tienen otros efectos, entre ellos la mejoría de la función endotelial, efecto precoz que resulta útil tras episodios coronarios agudos. Deben controlarse las enzimas (ALT, AST y CK).
Resinas de intercambio iononico. Son hipocolesterolemiantes menos intensos, que secuestran ácidos biliares y elevan la trigliceridemia.
Inhibidores selectivos de la absorción de colesterol. Ezetimibe inhibe específicamente la absorción de colesterol. Se usa en sustitución de estatinas o más frecuentemente en asociación con las mismas.
Fibratos. Son hipotrigliceridemiantes utilizados en hipertrigliceridemias, hiperlipidemias combinadas y situaciones con reducción de colesterol HDL.
Ácido nicotínico y asociación de niacina y lovastatina. El ácido nicotínico reduce triglicéridos y colesterol. Sus frecuentes efectos secundarios son mucho menores en la formulación de liberación controlada. Las asociaciones de estatinas a resinas, ezetimibe y fibratos pueden utilizarse (controlando enzimas en la asociación de estatinas y fibratos
Referencias:
Dorantes C. Y. Endocrinología Clínica, 3a Ed, Manual Moderno 2008, México
Hiperlipidemias primarias. Clasificación, diagnóstico y riesgo asociado A Mangas Rojas. R Toro Cebada. I Tinoco Racero. Medicine. 2008;10:1235-41.
Hiperlipidemias secundarias. Clasificaciones. Factores etiopatogénicos. Complicaciones. Valoración diagnóstica. Medicine 2008;10:1242-5
Incretinas en la Diabetes Mellitus tipo 2
Introducción
El tratamiento de la Diabetes Mellitus tipo 2 (DM2) es un reto para el médico, el poco apego del paciente a los medicamentos, la hipoglucemia y la ganancia de peso asociada a medicamentos anti-diabéticos son algunas de las variables que interfieren en el control glucémico del paciente.
Actualmente la terapéutica se ha centrado en aumentar la disponibilidad de la insulina a través de la administración de agentes orales que promuevan la secreción de insulina, disminuyan la resistencia periférica de esta y retrasen la absorción de carbohidratos a nivel gastrointestinal.
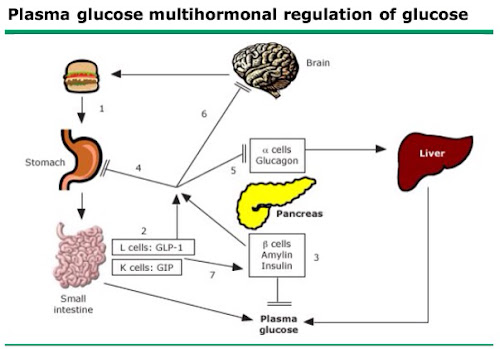
La homeostasis de la glucosa depende de el papel que juegan múltiples hormonas: Insulina, Amilina, Glucagon, GLP-1 (Glucagon-Like Peptide) y Polipéptido Insulinotrópico dependiente de glucosa (GIP: Gastric inhibitory polypeptide).
Revisemos el mecanismo de acción y la utilidad que tienen las incretinas en el tratamiento de la DM2.
Incretinas:
Las incretinas son hormonas producidas en el tracto gastrointestinal en respuesta a la ingesta de alimentos y con efecto sobre las células de los islotes de Langerhans, que aumentan la secreción y liberación de la insulina y disminuyen la secreción de glucagón dependiendo de la glucosa circulante. Las principales incretinas son el GLP1 y el GIP.
Efecto Incretina
El “efecto incretina” consiste en la mayor liberación de insulina por el páncreas cuando el estímulo de glucosa es gastrointestinal, comparado a cuando el estímulo es endovenoso. Este efecto está alterado en pacientes con diabetes tipo 2.
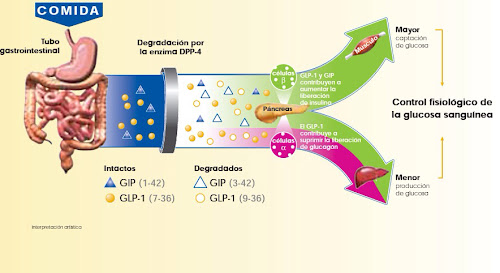
El efecto incretina se puede aumentar de dos formas: producir un GLP1 que no sea inactivado por DPP4, es decir, un análogo de GLP1; o inhibir a la enzima que desactiva a las incretinas mediante inhibidores de DPP4.
Glucagon-Like Peptide-1
El papel del GLP-1 en la homeostasis de la glucosa es representativo del efecto incretina, en el que la glucosa oral tiene un efecto estimulante sobre la secreción de insulina mayor que la glucosa intravenosa.
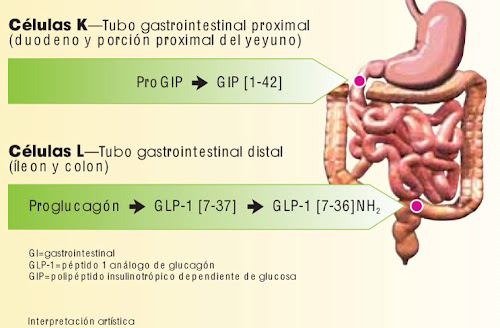
El GLP-1 es producido por el gen proglucagón en las células L del intestino delgado y se secreta en respuesta a los nutrientes. Los niveles de GLP-1 están disminuidos en la diabetes tipo 2 y la regulación de GLP-1 puede ser anormal en la diabetes tipo 1.
Efectos del GLP-1
Efecto principal: Estimula la liberacion de insulina glucosa-dependiente de los islotes pancreaticos.
Retrasa el vaciado gástrico
Inhibe la liberación de Glucagón
En modelos animales, el GLP-1 estimula la proliferación de las células beta.
El GLP-1 exhibe una vida media corta de uno a dos minutos debido a la degradación de su región N-terminal por la enzima dipeptidil peptidasa IV (DPP-IV).
GIP
Es secretado por las células K en la porción proximal del intestino (duodeno y yeyuno proximal). Estimula la liberación de insulina dependiente de la glucosa en las células beta.
Análogos del GLP-1
Exenatida
La exendina-4 es un componente natural de la saliva del monstruo de Gila (Heloderma suspectum), y comparte un 53% de la secuencia de aminoacidos con el GLP-1. Es resistente a la degradación de DPP-IV y por tanto exhibe una vida media prolongada (2-4 hrs)
Mecanismo de acción
In vitro, exenatida ha demostrado que se unen al receptor de GLP-1 de islotes de rata. La exenatida, como el GLP-1, se ha demostrado para promover la regeneración de las células beta y la diferenciación en las ratas prediabéticas y diabéticas.
La exenatida muestra una secrecion de insulina dosis-dependiente y glucosa-dependiente. Sus efectos insulinotropicos son suprimidos cuando la glucosa en plasma se acerca a 4 mmol / l (72 mg / dL). Al igual que el GLP-1, la exenatida retarda el vaciado gástrico,disminuye los niveles de glucagón, y ayuda a la pérdida de peso.
Efectos secundarios
- Los efectos secundarios de exenatide son fundamentalmente gastrointestinales.
- Hipoglucemias leves-severas cuando se administra con sulfonilureas.
Gastrointestinal:
- Nausea
- Perdida de peso
- Pancreatitis Aguda
Renal:
- Se han reportado algunos casos de IRA
Dosis: Esta disponible en jeringas precargadas con 5 o 10 mcg, se administra por via subcutanea 1 hr antes del desayuno y la cena.
No debe administrarse en pacientes con Enfermedad renal terminal.
Analogos del GLP-1 de accion prolongada.
Liraglutida
Analogo del GLP-1 que se administra una vez por semana (USA, Europa y Japon)
La Liraglutida es un análogo de GLP-1 que ha sido modificado para que se una a la albúmina sérica de manera no covalente a través de una cadena lateral de lípidos, lo que resulta en la degradación lenta y permitiendo una dosis semanal subcutánea. Está disponible para su uso como monoterapia como complemento de la dieta y el ejercicio o en combinación con agentes orales en adultos con diabetes tipo 2. No se considera una terapia de primera línea.
La dosis inicial es de 0,6 mg una vez al día durante una semana para reducir los efectos secundarios gastrointestinales. Después de una semana, la dosis debe aumentarse a 1,2 mg una vez al día durante una semana. Si glucosas sangre permanecen por encima del rango meta, la dosis se puede aumentar a 1,8 mg una vez al día.
Los eventos adversos más comunes son náuseas, vómitos y diarrea.
Exenatide de aplicacion semanal. (USA y Europa)
Inhibidores de DPP-IV
La Dipeptidil peptidasa IV (DPP-IV) es una enzima ubicua expresada en la superficie de la mayoría de tipos de células que desactiva una variedad de otros péptidos bioactivos, incluyendo GIP y GLP-1, por lo tanto, su inhibición podría afectar regulación de la glucosa a través de efectos múltiples, principalmente aumentando la vida media del GLP-1 endógeno.
Estos inhibidores, a diferencia de los analogos de GLP-1, se puede administrar por vía oral. La sitagliptina, saxagliptina y linagliptina son los inhibidores de la DPP-IV.
Los inhibidores de DPP-IV no son considerados como terapia inicial para la mayoría de los pacientes con diabetes tipo 2. Se pueden considerar como monoterapia en pacientes que no toleran o tienen contraindicaciones a la metformina, sulfonilureas o las tiazolidinedionas.
Sitagliptina
La sitagliptina es un inhibidor de DPP-IV, que está aprobado para el tratamiento de la diabetes tipo 2 (como monoterapia o como un segundo fármaco en aquellos que no responden a un solo agente, como una sulfonilurea, metformina o una tiazolidindiona, y como un tercer agente cuando la terapia dual con metformina y una sulfonilurea no proporcionan un control glucémico adecuado). La dosis habitual de sitagliptina es de 100 mg una vez al día, con reducción a 50 mg en IRC (TFG 30 a 50 ml / min) y 25 mg en IRC(TFG<30 ml / min).
La sitagliptina / metformina está disponible en una sola tableta (50 mg/500 mg y 50 mg/1000 mg)
Saxagliptina
Saxagliptina está aprobado como tratamiento inicial farmacológico para el tratamiento de la diabetes tipo 2, o como un segundo agente en aquellos que no responden a un solo agente, como una sulfonilurea, metformina o una tiazolidindiona. La dosis habitual de saxagliptina es de 2,5 o 5 mg una vez al día, la dosis de 2,5 mg se recomienda para pacientes con Enfermedad Renal (TFG≤ 50 ml / min) y para los pacientes que toman inhibidores del citocromo P450 3A4 / 5 (por ejemplo, ketoconazol).
Saxagliptina también es eficaz cuando se utiliza en combinación con metformina Saxagliptina / metformina está disponible en una sola tableta (5 mg/500 mg, 5 mg/1000 mg, 2,5 mg de mg/1000)
Vildagliptina
La vildagliptina es otro inhibidor de la DPP-IV disponible para su uso en algunos países, aunque no ha sido aprobado por la FDA. Es efectivo como monoterapia o en combinación con metformina, tiazolidinedionas o la insulina.
Linagliptina
Linagliptina está aprobado para su uso como adyuvante de la dieta y el ejercicio en adultos con diabetes tipo 2.
La dosis habitual de linagliptina es de 5 mg una vez al día, con o sin alimentos. Se elimina principalmente a través del sistema enterohepático. No requiere ajuste de dosis en pacientes con insuficiencia renal o hepática. Los inductores de CYP3A4 o de la glucoproteína P (por ejemplo, rifampicina) pueden disminuir la eficacia de linagliptina. Por lo tanto, los pacientes que requieren esos medicamentos deben recibir una alternativa a la linagliptina.